Kapitel 2
Övervakning – tidig diagnostik, progression och återfall
Cancerdiagnostik är en komplex process som, utöver den initiala kliniska misstanken, innefattar flera moment såsom radiologi, biopsier för morfologiska och molekylära analyser samt perifer provtagning inkluderande analys av biomarkörer för vissa maligna sjukdomar. De diagnostiska områden där biomarkörer används, eller har potential att användas, omfattar både screening innan cancer uppstår (cancerscreening) samt uppföljning efter en konstaterad cancerdiagnos.
NIH – National Cancer Institute definierar tidig diagnostik som identifiering av en sjukdom, såsom cancer, så snart de första tecknen och symtomen uppträder, för att underlätta behandling och/eller möjliggöra bot. Det relaterar till en beskrivning av cancer enligt TNM-stadieindelningssystemet för solida tumörer, där radiologiska undersökningar spelar en central roll. Med hjälp av stadieindelningen kan man skilja mellan tidig och avancerad/metastaserad cancer.
Tidig cancer är ett generellt begrepp som ofta inom solida tumörer syftar på cancer som inte hunnit sprida sig till andra delar av kroppen, där behandlingsintentionen ofta är kurativ. Det är dock viktigt att notera att vad som klassificeras som "tidig cancer" varierar mellan olika cancerformer.
Trots kurativt syftande behandling vid tidig cancer kvarstår vanligtvis en risk för att sjukdomen återkommer hos vissa patienter, det vill säga att ett recidiv uppstår. Återfallet kan vara lokalt, vid samma plats som den ursprungliga tumören (ipsilateralt), lokoregionalt (i närliggande vävnad eller lymfkörtlar) eller distalt, det vill säga i andra organ eller fjärrliggande lymfkörtlar. Beroende på typ och utbredning av återfallet kan målet med behandlingen förändras; vid förekomst av distala metastaser är syftet inte sällan palliativt. För vissa tumörformer finns dock fortfarande möjlighet till lång tids överlevnad eller bot även när sjukdomen diagnostiseras med distala metastaser initialt (de novo) eller efter kurativ syftande behandling, såsom vid testikelcancer där behandlingen vanligen ges med kurativ intention även vid spridd sjukdom.
Vid metastaserad sjukdom (stadium IV) sker uppföljningen för solida tumörer i regel med radiologiska metoder, främst datortomografi. Utifrån förändringar i metastasutbredning jämfört med initiala undersökningar bedöms sjukdomen som komplett remission (ingen synlig cancer på tidigare påvisade lokaler), stabil sjukdom (stable disease) eller progressiv sjukdom (progressive disease). Inom kliniska studier används ofta RECIST 1.1-kriterierna* för denna bedömning (se länk i källorna). Både tidig upptäckt av återfall och identifiering av sjukdomsprogression är avgörande för att kunna erbjuda optimal behandling och vägleda patienten i valet av nästa terapisteg.
Den här texten belyser hur biomarkörer stödjer eller kan stödja det kliniska arbetet inom screening, uppföljning och utvärdering av cancer.
Så kan biomarkörer användas
Användningsområden för biomarkörer kan delas in i följande kategorier:
- Cancerscreening
- Uppföljning efter behandling för tidig detektion av återfall
- Utvärdering av behandling vid metastaserad cancer
- Detektion av behandlingsprediktiva faktorer vid metastaserad cancer
a. Cancerscreening
De cancersjukdomar som har screeningsprogram som kan vara aktuella för den allmänna eller delar av befolkningen är: Bröstcancer, cervixcancer, kolorektalcancer och prostatacancer. Det finns även undantag som till exempel personer i befolkningen med ärftliga cancerpredispositionssyndrom, men den patientgruppen diskuteras inte i det här kapitlet.
- Bröstcancer: Mammografi är gold standard för screening. Det finns idag inga etablerade biomarkörer som har visat tillräcklig nytta för att ersätta eller komplettera mammografi.
- Cervixcancer: Screening bygger på cytologi (cellprov). Identifiering av onkogena HPV-typer (t.ex. 6, 11, 16, 18, 31, 33, 35, 39, 45, 51, 52, 58 och 59) betraktas som riskfaktor för utveckling av cervixcancer. Kolposkopi blir nästa steget i utredningen om onkogen HPV påvisas.
- Kolorektalcancer: År 2018 initierades införandet av nationell screening med fekalt immunkemiskt test (FIT/F-Hb), som detekterar små mängder blod i avföringen. Andra metoder, såsom multitarget
DNA- (mt-fDNA) och RNA-analyser (mt-fRNA) från avföring, har högre känslighet och jämförbar specificitet. Med hjälp av mt-fDNA analyseras bland annat KRAS-mutationer och metyleringsmönster
i NDRG och BMP3 samt β-aktin. Mt-fRNA analyserar transkript av åtta gener (ACY1, AREG, CDH1, EGLN2, KRAS, SMAD4 och TNSFRSF10B) som sedan normaliseras mot uttrycket av GAPDH mRNA.
Cf-DNA i blod har något lägre känslighet men liknande specificitet.
Tabell 1. I tabellen sammanfattas känslighet och specificitet för de olika screeningmetoderna för kolorektal cancerscreening.
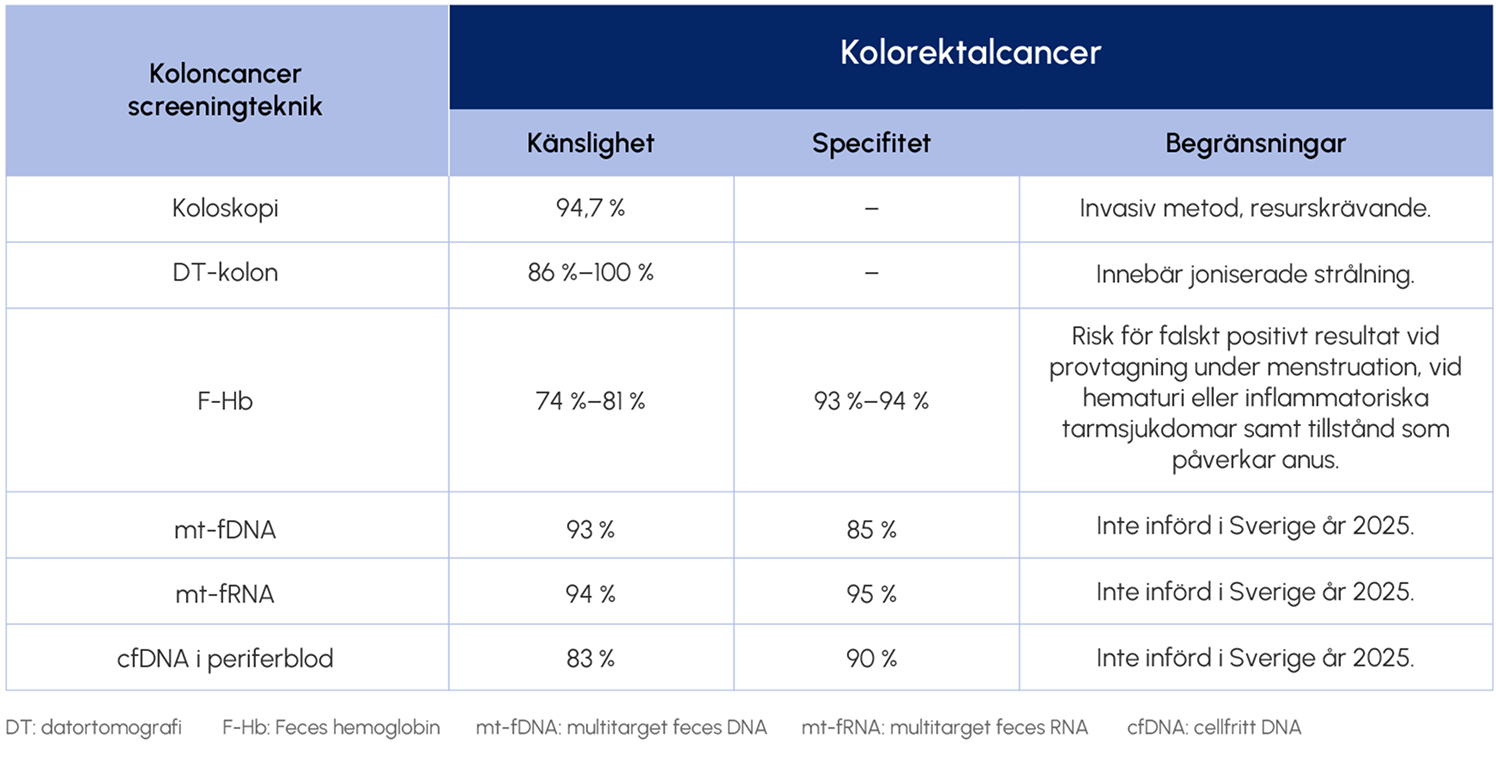
Källa: NCCN guidelines för colorectal cancer screening version 2.2025
- Prostatacancer: Prostataspecifikt Antigen (PSA) är den etablerade biomarkören. Befolkningsbaserad screening rekommenderas inte, då den riskerar att leda till överdiagnostik och överbehandling. Individbaserad screening kan övervägas efter informerat samtycke. 2025 publicerades en studie där polygenic risk score (PRS) via genetisk analys av material från blodprov kan möjliggöra selektion av individer med högre risk, vilket kan förändra framtida screeningsstrategier1
b. Uppföljning efter behandling av tidig cancer
Uppföljning sker oftast radiologiskt, med variation beroende på diagnos och stadium. Begreppet minimal residual disease (MRD) är etablerat inom hematologi, men utvärderas de senaste åren även vid solida tumörer via så kallad liquid biopsy vid vissa tumörsjukdomar. Förhoppningen med dessa metoder är att kunna identifiera återfall innan de kan ses med metoder som radiologi eller konventionella blodprover.
Analyser av MRD kan inkludera:
- Cirkulerande tumörceller (CTC)
- Cirkulerande tumör-DNA (ctDNA)
- Extracellulära nukleinsyror
Du kan läsa mer om CTC och ctDNA i Modul 3, kapitel 2 och 3.
Trots stora framsteg i förståelse är biologin bakom dessa biomarkörer inte är helt klarlagd vilket begränsar den kliniska nyttan av en sådan analys utanför kliniska studier.
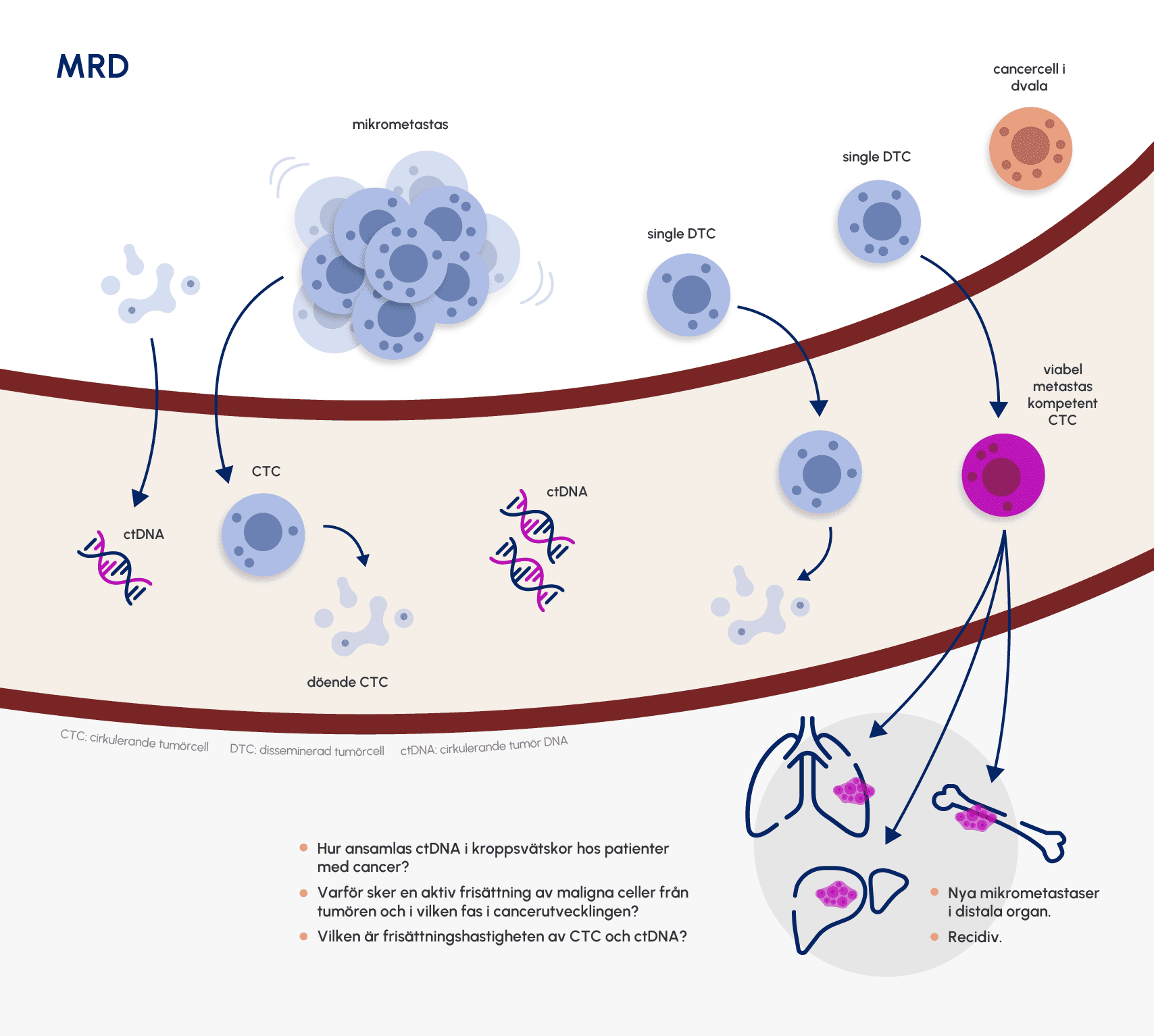
Figur 3. Figuren nedan sammanfattar biologin för MRD samt ännu obesvarade och avgörande frågor för implementering i klinisk vardag.
Anpassad efter: Pantel, K., Alix-Panabières, C. Minimal residual disease as a target for liquid biopsy in patients with solid tumours. Nat Rev Clin Oncol 22, 65–77 (2025). https://doi-org.ezproxy.its.uu.se/10.1038/s41571-024-00967-y
Exempel på etablerade biokemiska biomarkörer för uppföljning:
- Tyreoideacancer: Tyreoglobulin (differentierad cancer), kalcitonin och CEA (medullär cancer)
- Testikelcancer: AFP, β-HCG och LD (enligt rekommendationen från den Swedish and Norwegian testicular cancer group- SWENOTECA)2
- Prostatacancer: PSA
- Hepatocellulär cancer: AFP parallellt med radiologisk kontroll
- Kolorektalcancer: CEA rekommenderas postoperativt vid stadium II–III, vid 12 och 36 månader efter operation, som komplement till CT.
c. Utvärdering av behandling vid metastaserad cancer
Den huvudsakliga metoden är radiologisk utvärdering. Samma biomarkörer som används vid uppföljning av tidig cancer kan komplettera denna bedömning. För differentierad tyreoideacancer har tyreoglobulin särskilt värde.
d. Detektion av behandlingsprediktiva faktorer vid metastaserad cancer
Antalet behandlingsprediktiva biomarkörer har ökat kraftigt och diskuteras inom ramen för precisionsmedicinsk behandling.
Författare: Evangelos Digkas, MD, BSc, PhD, oktober 2025. Läs mer om författaren »
Källor
- McHugh JK, Bancroft EK, et al; BARCODE1 Steering Committee and Collaborators. Assessment of a Polygenic Risk Score in Screening for Prostate Cancer. N Engl J Med. 2025;392(14):1406-1417. doi: 10.1056/NEJMoa2407934.
- https://www.swenoteca.org
Fördjupad läsning
Imperiale TF, Porter K, et al; BLUE-C Study Investigators. Next-Generation Multitarget Stool DNA Test for Colorectal Cancer Screening. N Engl J Med. 2024;390(11):984-993. doi: 10.1056/NEJMoa2310336.
Barnell EK, Wurtzler EM, et al; Multitarget Stool RNA Test for Colorectal Cancer Screening. JAMA. 2023 Nov 14;330(18):1760-1768. doi: 10.1001/jama.2023.22231. Erratum in: JAMA. 2024;331(10):888. doi: 10.1001/jama.2024.1637.
Chung DC, Gray DM 2nd, et al; A Cell-free DNA Blood-Based Test for Colorectal Cancer Screening. N Engl J Med. 2024;390(11):973-983. doi: 10.1056/NEJMoa2304714.
SWE-NP-0725-80012
*RECIST 1.1 är radiologiska kriterier som baseras på anatomiska egenskaper på sjukdomen och är relevanta för de flesta solida maligna diagnoser men inte för alla. Det finns anpassande versioner för några diagnoser såsom för mesoteliom (mRECIST) samt för immunterapi (tex irRECIST). De kan inte användas för att bedöma hematologiska maligna sjukdomar där andra kriterier gäller som Lugano kriterier för lymfom.


